আইসোটনিক এবং হাইপার্টনিকের মধ্যে পার্থক্য | Isotonic বনাম হাইপার্টনিক
কী পার্থক্য - Isotonic বনাম Hypertonic
isotonic এবং hypertonic মধ্যে পার্থক্য বিশ্লেষণ আগে Tonicity ধারণা বুঝতে গুরুত্বপূর্ণ। অতএব, আমাদের প্রথমে টনিসটিটির ধারণা এবং এর গুরুত্বকে সংক্ষিপ্তভাবে বর্ণনা করা যাক। টনিসাইটিটি হল দুটি সমাধান জল সেন্সর মধ্যে বিভক্ত একটি semipermeable ঝিল্লি দ্বারা বিভক্ত। এটি আপেক্ষিক জল ঘনত্ব হিসাবে ব্যাখ্যা করা যেতে পারে যা ঝিল্লির উভয় পাশে সমান পরিমাণে সমান পরিমাণে পৌঁছানো পর্যন্ত পানি এবং দূরত্বের পরিমাণ নির্ধারণ করে। সমাধান টনিসিটি সনাক্তকরণ দ্বারা, আমরা নির্ধারণ করতে পারেন যে কোন দিকের জল বিক্ষিপ্ত হবে। একটি বহিরাগত সমাধান মধ্যে নিমজ্জিত কোষ প্রতিক্রিয়া illustrating যখন এই ঘটনাটি সাধারণত ব্যবহার করা হয়। টনিসটিটির তিনটি শ্রেণীবিন্যাস রয়েছে যা এক সমাধান অন্যের আপেক্ষিক হতে পারে। তারা হাইপার্টনিক, হাইপোটোনিক, এবং আইসোটনিক। মূল পার্থক্য Isotonic এবং Hypertonic মধ্যে যে হাইপার্টনিক সমাধান solute তুলনায় আরো দ্রাবক রয়েছে যখন solute এবং দ্রাবক সমান সমান সমাধান in isotonic সমাধান। তবে, হাইপোনিক ও হাইড্রোনিকিক সমাধানগুলির মধ্যে পার্থক্যটি যদি আমরা বুঝতে পারতে পারি তবে হাইপারটনিক ও আইসোটনেটিক সমাধানের কথা স্মরণ করা অপরিহার্য নয়।
হাইপার্টনিক কি?
উপরে বা অত্যধিক জন্য হাইপার আরেকটি শব্দ। হাইপারটনিক সমাধান সেলের চেয়ে সলিউশন (গ্লুকোজ বা লবণ) এর উচ্চতর ঘনত্ব থাকবে। Solutes হল একটি দ্রাবক মধ্যে দ্রবীভূত উপাদান, যার ফলে একটি সমাধান গঠন। একটি হাইপারটনিক সমাধান ইন, solutes এর ঘনত্ব তার ভিতরে ভিতরে কোষ বাইরে বড়। যখন একটি কোষ হাইপারটনিক সমাধানে নিমজ্জিত হয় তখন একটি অজোমটিক স্থানান্তরিত হবে এবং ঘন ঘন ঘনত্বের ভারসাম্য বজায় রাখতে এবং কোষের আকারে সংকোচন হবে।
Isotonic কি?
ইএসও সমান এবং টনিকের জন্য আরেকটি শব্দ হল সমাধানটির টনিসটিটি। Isotonic সমাধান এটি তুলনা করা হচ্ছে এর সমাধান চেয়ে solute অনুরূপ ঘনত্ব হবে। একটি isotonic সমাধান ইন, solutes এর ঘনত্ব সেলুলার প্রতিষ্ঠানের পরিবেশের মধ্যে একটি ভারসাম্য তৈরি সেল এর ভিতরে এবং বাইরে উভয় একই। একটি কোষ একটি isotonic সমাধান নিমজ্জিত করা হয় যখন, solutes এর ঘনত্ব ভারসাম্য উভয় নির্দেশের মধ্যে কোষ ঝিল্লি মাধ্যমে একটি osmotic স্থানান্তর এবং জল অণুগুলি থাকবে না।এই প্রক্রিয়াটি কোষের স্নায়ু বা সংকোচনের সৃষ্টি করবে না।

Isotonic এবং Hypertonic মধ্যে পার্থক্য কি?
হাইপারটোনিক এবং আইসোটোনিকের মধ্যে পার্থক্যগুলি নিম্নবর্ণিত শ্রেণিতে শ্রেণীবদ্ধ করা যায়।
সংজ্ঞা আইসোটোনিক এবং হাইপার্টনিক
হাইপার্টনিক: "হাইপার" উপরে বা অত্যধিক হিসাবে পরিচিত হয় + "টনিক" একটি সমাধান এর লাইন বরাবর কিছু হিসাবে পরিচিত হয়। এইভাবে, হাইপারটনীয় সমাধান এর বৃদ্ধি tonicity প্রস্তাবিত।
Isotonic: "আইওও" একই নামে পরিচিত "+ টনিক" একটি সমাধান লাইন বরাবর কিছু হিসাবে পরিচিত হয়। সুতরাং, isotonic সমাধান অনুরূপ tonicity প্রস্তাব দেওয়া হয়।
বৈশিষ্ট্যসমূহ এসোটিনিক এবং হাইপার্টনিক
সলিউশন এবং সমাধানের সঞ্চার করুন
হাইপার্টনিক: সলিউশন সলিউটের চেয়ে বেশি দ্রাবক রয়েছে।
আইজোটনিক: সমাধানে দ্রাবক এবং দ্রাবকটি একটি সমানভাবে বিতরণ করা হয়।
উদাহরণ
হাইপার্টনিক: শুদ্ধ পানি, কারন শুদ্ধ পানি কোন দ্রব্যে দ্রবীভুত হয় না এবং সেলুলার পরিবেশের তুলনায় এটির ঘনত্ব খুবই কম।
এসোটিনিক: লবণাক্ত সমাধান হল মানুষের রক্তের রক্তস্রাবের জন্য একটি যৌগ।
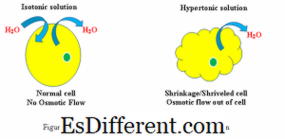
hypertonic এবং isotonic সমাধান সেলগুলির প্রতিক্রিয়া (চিত্র 1 দেখুন)
হাইপার্টনিক: যখন একটি জৈবিক কক্ষ থাকে হাইপারটনীয় পরিবেশ, কোষের বাইরে কোষের ঝিল্লি জুড়ে পানি প্রবাহিত হয়, যাতে কোষের ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘনত্ব ফলস্বরূপ, সেলটি সঙ্কুচিত হবে কারণ বাইরের পরিবেশে সলিউশনের উচ্চতর ঘনত্ব কমাতে কোষটি কোষে ফেলে দেয়।
আইজোটনিক: যখন একটি কোষ অ্যাসোসিয়েটিক সমাধানে থাকে, তখন কোষের ফোলা বা সঙ্কোচন করা হবে না।
জল সেন্স্রেটেশন গ্রেডিয়েন্ট
হাইপার্টনিক: হাইপারটনিক সমাধান থেকে ঘরের ভিতর থেকে জল সেন্স্রেশন গ্রেডিয়েন্টটি দেখা যায়ঃ এসোটিনিক:
জল সেন্স্রেশন গ্রেডিয়েন্ট বিদ্যমান নয় সলিট সেন্সেন্টেশন গ্রেডিয়েন্ট < হাইপার্টনিক:
ঘন ঘন ঘনত্বের ঘনত্ব কোষের ভিতরের হাইপার্টনিক সমাধান থেকে দেখা যায়
আইজোটনিক: কঠিন সন্নিবেশ গ্রেডিয়েন্টটি বিদ্যমান নয়।
অসমোটিক স্থানান্তর হাইপার্টনিক:
অজোমটিক শিফ্টটি বিদ্যমান।
আইজোটিকিক: অজোমটিক শিলা বিদ্যমান নয়
জল আন্দোলন হাইপার্টনিক:
কোষের বাইরের সমাধান দিক থেকে পানি অণুটি দ্রুত সরানো বা ছড়িয়ে পড়ে, এবং এইভাবে কোষটি পানি হারাবে ।
আইসোটনিক: পানির অণু উভয় দিক দিয়ে সরানো বা প্রবাহিত হয় এবং পানি সংশ্লেষের হার প্রতিটি দিকের অনুরূপ। সুতরাং কোষটি প্রাপ্ত হবে বা পানি হারাবে।
স্পোর্টস ড্রিংক আইসোটনিক:
একটি আইসোটোনিক পানীয় মানুষের শরীরের মতো লবণ, চিনির কার্বোহাইড্রেট এবং ইলেক্ট্রোলাইটের সমতুল্য। Isotonic স্পোর্টস পানীয় প্রায়ই একটি মৌখিক পুনর্ব্যবহারযোগ্য সমাধান হিসাবে পছন্দ করা হয়। এটি সাধারণত প্রতি 100 মিলি প্রতি 4-8 গ্রাম কার্বোহাইড্রেট থাকে।
হাইপার্টনিক: হাইপারটনিক পানীয় লবণ, চিনির কার্বোহাইড্রেট এবং ইলেক্ট্রোলাইটের উচ্চ পরিমাণে মানুষের দেহে যেমন থাকে।এটি সাধারণত প্রতি 100 মিলি প্রতি 8 গ্রাম কার্বোহাইড্রেট থাকে। সেরিব্রাল রক্তক্ষরণ পরিচালনার জন্য একটি হাইপার্টনিক সমাধান osmotherapy ব্যবহার করা হয়। Hypertonic ক্রীড়া পানীয় যারা উচ্চ মাত্রার শক্তি প্রয়োজন জন্য আদর্শ।
উপসংহারে, দ্রাবক ঘনত্বের উপর ভিত্তি করে সমাধানগুলির তিনটি ধরণ আছে এবং এটি হল isotonic, হাইপোটনিক এবং হাইপার্টনিক। সলিউশনের ঘনত্ব ইস্ট্রোনিক সমাধানের ভেতর ও বাইরের উভয়েরই সমান। কোষের ঘনত্ব হিপোটনিক সমাধানের বাইরের পরিবেশের তুলনায় কোষের ভিতরে অধিকতর হয়, তবে হাইপারটনিক সমাধান এমন এক যেখানে ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন ঘন পরিবেশের চেয়ে বেশি নয়। রেফারেন্স মনসুর, এম। এ।, বেভারলি, জে।, এবং স্যান্ডম্যান। (2002)। ফার্মেসী বিভাগ দ্বারা ম্যাকগ্রা-হিল পেশাদার পিপি 54-57 ভয়েট, ডি।, জুডিথ, জি। ভি। এবং শার্লট, ডব্লু পি। (2001)। বায়োকেমিস্ট্রি (রেভ। এড।) এর মূলধন নিউ ইয়র্ক: উইলি পি। 30. চিত্র সৌজন্যে: LadyofHats দ্বারা "রক্ত কোষ ডায়াগ্রামে অসমোটিক চাপ" - এটি কি উইকিমিডিয়া কমন্স দ্বারা [1], [2], [3] এবং [4] … (পাবলিক ডোমেন) উপর ভিত্তি করে তৈরি করেছে



