মনোটোমিক এবং ডায়োটমিকের মধ্যে পার্থক্য | Monatomic বনাম Diatomic
মনোটোমিক এবং ডায়োটোমিকের মধ্যে পার্থক্য প্রাথমিকভাবে প্রজাতির মধ্যে থাকা পরমাণুগুলির সাথে। নামগুলি উল্লিখিত, উভয় এই পদগুলি পারমাণবিক সংস্থার বিভিন্ন রাজ্যগুলির জন্য দাঁড়িয়ে আছে যেখানে 'মোনো' মানে 'এক' এবং 'দ্বি' অর্থ 'দুটি। 'অতএব, একমাত্র অর্থোপযোগী অর্থ এক'
এক পরমাণু 'ডায়োটমিক মানে' দুটি পরমাণু। ' যাইহোক, এই মৌলিক সংজ্ঞা থেকে অনেক ভিন্ন ভিন্নতা থাকতে পারে।
মনোটোমিক কি?কখন
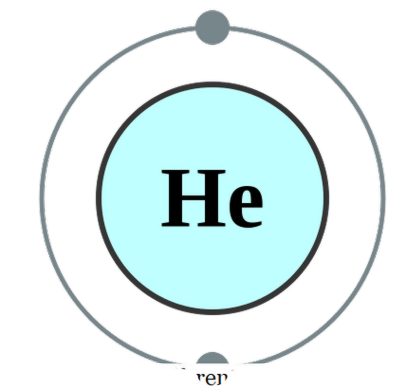
একক পারমাণবিক অস্তিত্ব তার নিজস্ব (যা খুব কম ক্ষেত্রেই) বিদ্যমান, আমরা এটি monatomic বলি। এই উপাদান তাদের বিশুদ্ধ একবচন ফর্ম মধ্যে মানে। এই বিভাগের অধীনে আসতে পারে এমন একমাত্র বাস্তব উদাহরণটিই হবে উত্তম গ্যাস যা তাদের পরমাণু হিসাবে বিদ্যমান থাকবে যেমনটি তাদের ইলেকট্রনের একটি অক্টেটের সাথে সম্পন্ন হয়েছে। তাই, আরো স্থিতিশীল হওয়ার জন্য তারা কোনও ইলেকট্রন গ্রহন বা গ্রহন করার চেষ্টা করে না। অতএব, উত্তম গ্যাস monatomic ফর্ম স্থিতিশীল হয়। কিছু উদাহরণ; তিনি - হিলিয়াম, নে - নিওন, আর - আর্গন, জি - জিনন, ক্র - ক্রিপটন, আরএন - রাডন।
ডায়োটমিক কি?
কখন
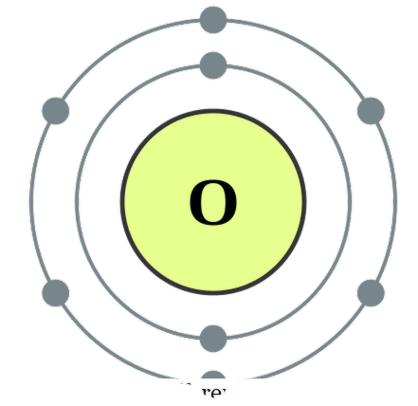
দুই পরমাণু একে অপরের সাথে মিলিত হয় , আমরা ডায়োটমিককে কল করি। এই পরমাণুগুলি একই ধরনের হতে পারে বা ভিন্ন হতে পারে। যখন তারা দুটি সমতুল্য হয় তখন আমরা ' হোমোনিউরনিক ডায়্যাটমস ' এবং এটির বিভিন্ন ধরণের তৈরি করা হলে আমরা এটি ' হেটোনারিকাল ডায়োটোমস ' 'বলে থাকি। কিছু হোমোনিউরিয়র ডায়্যাটোমের উদাহরণগুলি O2, N2, H2 ইত্যাদি হতে পারে। তবে কোও, না, এইচএলসি ইত্যাদি হাইটোনিওনিক ডায়্যাটোমের উদাহরণ হিসাবে দেওয়া যেতে পারে। অক্সিজেন
ডায়োটোমগুলি যৌগ হিসেবে বিবেচনা করা যেতে পারে কারণ তারা একে অপরের সাথে ইলেক্ট্রন ভাগ করে আরো স্থিতিশীলতা লাভ করার জন্য এই সংস্থার গঠন করে যাতে উভয় পরমাণু উত্তম গ্যাস ইলেকট্রনিক কনফিগারেশন অর্জন করে। তারা পারমাণবিক অরবিটলের ওভারল্যাপিং দ্বারা সহস্রাব্দ বন্ডের মাধ্যমে বন্ড বা অন্যথায় তারা তাদের মধ্যে ionic বন্ধন গঠন করতে পারে যা একটি ইতিবাচক চার্জযুক্ত প্রজাতি এবং একটি নেতিবাচক চার্জযুক্ত প্রজাতির মধ্যে একটি আকর্ষণ বল। ডায়্যাটম মধ্যে সহস্রাব্দ বন্ডের উদাহরণ CO, NO, ইত্যাদি অন্তর্ভুক্ত এবং এইচএলসি একটি আইওনিক আকর্ষণ চরিত্রের সাথে প্রজাতি হিসাবে বিবেচনা করা যেতে পারে। যাইহোক, এইচ + এবং ক্লি-এর মধ্যে আকর্ষণের বাহনটি খুব শক্তিশালী নয়, এটি আইওনিক বন্ডগুলির জন্য একটি ভাল উদাহরণ নয় যা অন্য একটি নির্দিষ্ট বিষয়।
মনোটোমিক এবং ডায়োটমিকের মধ্যে পার্থক্য কি?
• ডায়োটমিক প্রজাতির দুটি পরমাণু থাকলে মনোটোমিক প্রজাতির একটি এ্যাটম থাকে।
• মনোটোমিক প্রজাতি সাধারণত স্থিতিশীল নয়, তবে ডায়োটোমিক প্রজাতিটি সাধারণত স্থিতিশীল।
• নোবল গ্যাসগুলি কেবলমাত্র monatomic এবং diatomic আকারে পাওয়া যায় না।
• ডায়োটমিক প্রজাতির মধ্যে রাসায়নিক বন্ধন বিদ্যমান থাকলেও monatomic প্রজাতির কোন বন্ধন নেই।
চিত্র সৌজন্যে:
পাম্বা দ্বারা হিলিয়াম ইলেক্ট্রন কনফিগারেশন (সিসি বাই-এসএ 2. 0 ইউ)
- ডিপিপের মাধ্যমে অক্সিজেন ইলেক্ট্রন কনফিগারেশন (সিসি বাই-এসএ 3. 0)




