এস এবং পি ব্লক উপাদানগুলির মধ্যে পার্থক্য | এস বনাম পি ব্লক উপাদানসমূহ
কী পার্থক্য - এস পি ব্লক উপাদানসমূহ
কী পার্থক্য s এবং p ব্লক উপাদানগুলির মধ্যে তাদের ইলেকট্রনিক কনফিগারেশন ব্যবহার করে সর্বোত্তমভাবে ব্যাখ্যা করা যায়। ব্লক উপাদানগুলির মধ্যে, শেষ ইলেকট্রনটি s subshell এবং p ব্লক উপাদানগুলিতে পূর্ণ করে, শেষ ইলেকট্রন পি subshell এ ভর্তি হয়। যখন তারা আয়ন গঠন; এর ব্লক উপাদান সহজে বাইরের সর্বাধিক subshell থেকে তাদের ইলেকট্রনগুলি সরাতে পারে যখন পি ব্লক উপাদান পি subshell ইলেক্ট্রন গ্রহণ বা পি - subshell থেকে ইলেকট্রন অপসারণ। প-গ্রুপের কিছু উপাদান বাইরের সর্বাধিক প-সাবসেলে ইলেকট্রনগুলি সরিয়ে দেয় এবং কিছু উপাদান (সবচেয়ে ইলেকট্রনগাটিভ উপাদান) অন্য একটি থেকে ইলেক্ট্রন গ্রহন করে নেতিবাচক আয়ন গঠন করে। আপনি যখন রাসায়নিক বৈশিষ্ট্যগুলি বিবেচনা করেন তখন s এবং p ব্লক উপাদানগুলির মধ্যে একটি উল্লেখযোগ্য পার্থক্য রয়েছে; এই মূলত ইলেকট্রন কনফিগারেশন কারণে।
এস ব্লক উপাদানগুলি কি?
S- ব্লক উপাদানগুলি পর্যায় সারণিতে গ্রুপ I এবং গ্রুপ II মধ্যে রাসায়নিক উপাদান। যেহেতু এস subshell শুধুমাত্র দুটি ইলেকট্রন মিটমাট করতে পারে, তাই এই উপাদানে সাধারণত বাইরের সর্বোচ্চ শেলের মধ্যে একটি (গ্রুপ I) বা দুটি (গ্রুপ II) ইলেকট্রন থাকে। গ্রুপ I এবং II- এর উপাদানগুলি টেবিলের উপরে দেখানো হয়।
- টেবিল থেকে প্রান্তিক প্রান্তিক মধ্যম ->| আইএ | ২000 এ | |
| ২ | লি | বে |
| 3 | না | এমজি |
| 4 | কে | ক্যাচ |
| 5 | RB | সিনিয়র |
| 6 | Cs | Ba থেকে |
| 7 | ফরাসী ভাষায় | রা |
| আইএ | ক্ষার ধাতু |
| ২008 এ | ক্ষারীয় পৃথিবী ধাতব |
এস-ব্লকের সমস্ত উপাদান ইতিবাচক আয়ন এবং তারা খুব প্রতিক্রিয়াশীল।
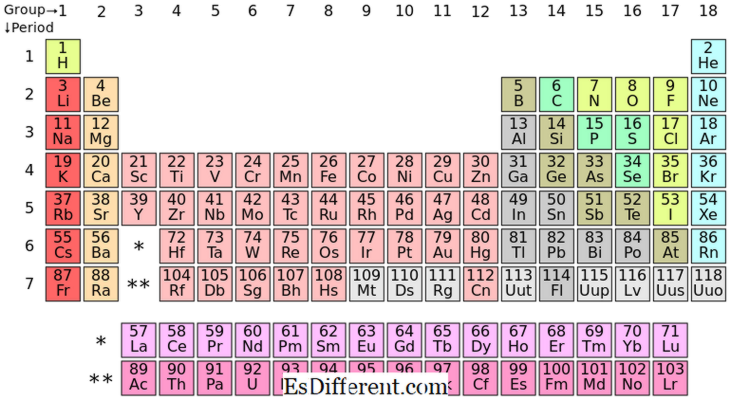
পর্যায়ক্রমিক সারণিতে S- ব্লক উপাদানগুলির অবস্থান নির্ধারণ
পি ব্লক উপাদান কি?
পি-ব্লক উপাদানগুলি হল এমন উপাদান যা শেষ ইলেকট্রন পি সাশেলে পূরণ করে। তিনটি p-orbitals আছে; প্রতিটি কক্ষপথ দুটি ইলেকট্রন মিটমাট করতে পারে, যার ফলে ছয়টি ইলেক্ট্রন তৈরি হয়। অতএব, পি-ব্লক উপাদানগুলি তাদের বাইরের সর্বাধিক শেলের মধ্যে ছয়টি পি-ইলেকট্রন রয়েছে। P- ব্লক ধাতু এবং অ ধাতু উভয় অন্তর্ভুক্ত; উপরন্তু কিছু metalloids আছে খুব।
| 13 | 14 | 15 | 16 | 17 | 18 | |
| 2 | b | সি | এন | হে | এফ নে | 3 |
| আল | যদি | পি | এস | যোগাযোগ Cl | আরবীতে | 4 |
| গা | Ge থেকে | হিসাবে | Se থেকে | ব্রাউ | Kr | 5 |
| সালে | Sn | Sb | আপনি এখানে | আমি | Xe | 6 |
| TL | Pb বি | পো | এ | Rn | এস এবং পি ব্লক উপাদানগুলির মধ্যে পার্থক্য কি? | সাধারণ ইলেক্ট্রন কনফিগারেশন: |
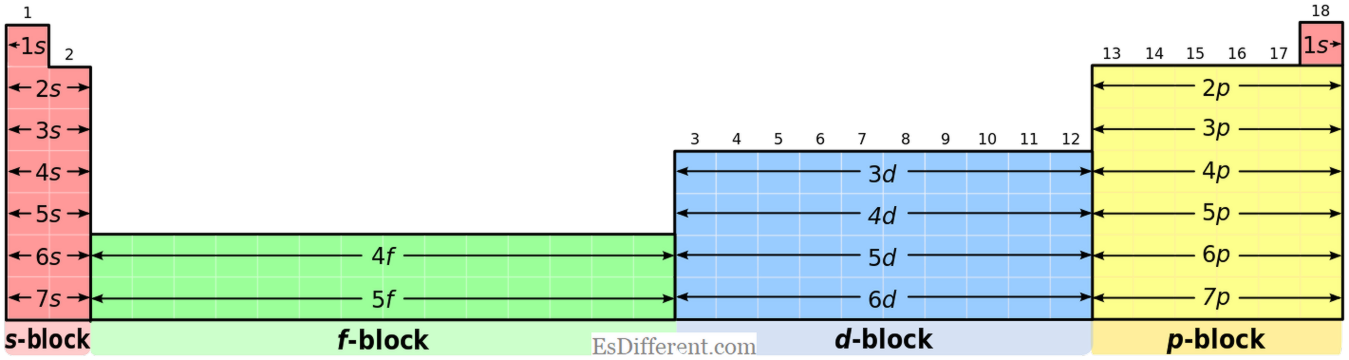
S- ব্লক উপাদান:
S- ব্লক উপাদানগুলি [উত্তম গ্যাস] ns
1 (গ্রুপ I উপাদানগুলির জন্য) এবং [উত্তম গ্যাস] ns 2 (গ্রুপ II উপাদানের জন্য)। পি-ব্লক উপাদানসমূহ: পি-ব্লক উপাদানগুলি [উত্তম গ্যাস] ns
2 np 1-6 এর সাধারণ ইলেক্ট্রন কনফিগারেশন আছে। কিন্তু, হিলিয়াম এর 1s 2 কনফিগারেশন; এটি একটি বিশেষ পরিস্থিতি। জারণ রাজ্যঃ S- ব্লক উপাদানসমূহ:
S- ব্লক উপাদানগুলি একাধিক অক্সিডেশন রাষ্ট্র যেমন পি-ব্লক উপাদান দেখায় না। উদাহরণস্বরূপ, গ্রুপ I উপাদানগুলি +1 অক্সিডেশন স্টেট দেখায় এবং গোষ্ঠী ২ টি উপাদান +2 অক্সিডেশন স্টেট দেখায়।
পি-ব্লক উপাদানসমূহ: এস-ব্লক উপাদানের পরিবর্তে, পি-ব্লক উপাদানগুলি আঞ্চলিক টেবিল এবং আয়নের স্থিতিশীলতার উপর নির্ভর করে কিছু অন্যান্য অতিরিক্ত অক্সিডেশন স্টেটগুলিতে নিজ নিজ গোষ্ঠীর জন্য একটি সাধারণ অক্সিডেশন রাষ্ট্র রয়েছে।
গ্রুপ 13
| 14 | 15 | 16 | 17 | 18 | সাধারণ ইলেক্ট্রন কনফিগারেশন | ns |
| 2 | np 1 NS 2 | NP 2 NS 2 | NP 3 NS 2 | NP 4 এনএস ২ এনপি | 5 এনএস ২ এন পি | 6 1 স্ট গ্রুপের সদস্য |
| সি এন ও | ফল | তিনি | সাধারণ অক্সিডেসন সংখ্যা | +3 | +4 | +5 |
| -2 | -1 | 0 | অন্যান্য অক্সিডেশন যুক্তরাষ্ট্র | +1 | +2, -4 | +3, -3 |
| +4, +2, | +3, +5, + 1, +7 | - | বৈশিষ্ট্যাবলী: | এস-ব্লক উপাদানসমূহ: | সাধারণভাবে, সমস্ত S- ব্লক উপাদান হল ধাতু। তারা চকচকে, ভাল বৈদ্যুতিক এবং তাপ কন্ডাক্টর এবং ভ্যালেন্স শেল থেকে ইলেকট্রন সরানো সহজ। তারা পর্যায় সারণিতে সবচেয়ে প্রতিক্রিয়াশীল উপাদান। | পি-ব্লক উপাদান: |
অধিকাংশ পি-ব্লক উপাদান অ ধাতু-ধাতু। তারা কম উত্থাপন পয়েন্ট, দরিদ্র conductors এবং বাইরের সর্বোচ্চ শেল থেকে ইলেকট্রন অপসারণ কঠিন। পরিবর্তে, তারা ইলেকট্রন লাভ। কিছু অ ধাতবগুলি কক্ষ তাপমাত্রায় সলিড (সি, পি, এস, সে) হয় এবং কিছু গ্যাস (অক্সিজেন, নাইট্রোজেন) হয়। ব্রোমাইন একটি অ ধাতু, এবং এটি কক্ষ তাপমাত্রায় একটি তরল।
উপরন্তু, পি-ব্লক কিছু ধাতব উপাদান রয়েছে; অ্যালুমিনিয়াম (আল), গ্যালিয়াম (গা), ইণ্ডিয়ম (ইন), টিন (এসএন), থ্যালিয়াম (টিএল), সীসা (পিবি), এবং বিস্মিত (দ্বি)। চিত্র সৌজন্যে:
1 DePiep দ্বারা "পর্যায়ক্রমিক সারণি (বহুমাত্রিক)" [সিসি বাই-এসএ 3। 0] কমন্স দ্বারা ২। "পর্যায়ক্রমিক টেবিল ব্লক SPDF (32 কলাম)" ব্যবহারকারী দ্বারা: ডিপিআইপি [সিসি বাই-এসএ 3। 0] কমনস:




